執筆:石曽根隆(東京工業大学)
高分子の分子量、分子量分布を迅速に測定できる最も一般的な分析手段
ゲル濾過クロマトグラフィー(gel permeation chromatography: GPC)は、高速液体クロマトグラフィー(high performance liquid chromatography: HPLC)の一種であり、溶媒中における高分子のサイズ(分子量)の違いに由来して多孔質のカラム固定相への保持時間(retention time)の違い(分離)が生じることで、高分子の分子量、分子量分布の測定が可能です。高分子の分子量変化を伴う反応の追跡や分取(分子量分割)にも用いられます。
測定できること
分子量 / 分子量分布 / 分子量変化 / 化学構造変化 / 相対分子量 / 絶対分子量 / 分取GPC
原理
GPC(gel permeation chromatography、ゲル浸透クロマトグラフィー)は、高速液体クロマトグラフィー(HPLC)の一種であり、分離に用いられる担体に大きな特徴があり、現在、合成高分子や生体高分子の分子量や分子量分布測定に幅広く用いられています。有機化学や生化学で用いられる順相や逆相HPLCでは、測定対象分子群とカラム担体(または溶媒)との化学的な親和性、相互作用の差を利用して分子を分離させますが、GPCでは、高分子のサイズ(分子量に基づく流体力学体積)の違いによって分離を行うことが特徴となります。その測定原理から、GPCはサイズ排除クロマトグラフィー(SEC:size exclusion chromatography)とも呼ばれることも多くなっています。
有機溶媒系GPCでは、典型的なカラム固定相としてスチレンと
p-ジビニルベンゼンの共重合によって得られた多孔質の架橋体ゲルが用いられます。カラム内に充填されたビーズ状ポリスチレンゲルには細孔が多数存在し、溶質である高分子は溶液中での分子サイズによってその細孔に浸透(permeation)することを繰り返しながら溶媒の流れに従って移動します。図1に示すように、サイズが大きな分子は、細かな孔には浸透できずに、ゲルの間をすり抜けて早く溶出されます。一方、サイズが小さな分子は、細孔の奥にまで入り込み、溶出に時間が掛かることになります。それらの結果として分子量の大きな分子ほど早く溶出し、分子量の小さな分子ほど遅く溶出することとなり、分子量やその分布がクロマトグラムとして得られます。一方、水系GPCではシリカ系充填剤やデキストリンゲルなどがカラム固定相として使用され、高極性のポリエチレングルコールやタンパク質など生体高分子の分子量測定に用いられます。
.jpg) 図1 多孔性GPCゲルにおける分離の模式図
図1 多孔性GPCゲルにおける分離の模式図
典型的なGPC装置の構成を図2に示します。基本的にはHPLC装置にGPCモードで分離ができるカラムを取り付けてあり、測定精度、再現性を高めるためにはカラムオーブン、溶媒の脱ガス装置を併用することが望ましくなっています。検出器には、示差屈折率検出器(RI)や紫外吸光検出器(UV)が広く用いられ、溶出時間ごとの試料濃度を求めることができます。まず、溶媒、ポンプ流量、温度、カラムの種類と本数が一定の条件下、分子量が既知の標準試料(ポリスチレン、ポリエチレングルコール、プルランなど)を分子量領域を変えて測定し、分子量と溶出時間(retention time、または溶出体積)の較正曲線(calibration curve、検量線)を作成します(図3)。続いて、同条件下で未知試料を測定し、各溶出時間と較正曲線から分子量を算出します。この方法によって求められた分子量は、標準試料を元に測定試料の分子量を相対的に算出することから、相対分子量(relative molecular weight)と呼ばれます。基本的に較正曲線の傾きが小さい領域ほど分解能が高いことになります。図2に示したように、GPC検出器に光散乱検出器(LS)や粘度検出器(viscosity)を併用することで、絶対分子量(absolute molecular weight)の測定も可能となります。
GPCは基本的にクロマトグラフィーであることから、分子量解析以外に、分子量による分割、重合度に応じた単離、精製にも使用できます。分析用GPCのカラム径は0.6センチ程度ですが、分取GPCの場合には、大容量の送液ポンプと大口径(2-4センチ)カラムが用いられ、比較的大量のポリマー試料を注入して分子量(オリゴマーの場合は重合度)に基づく分離、精製を行うことが可能となります。
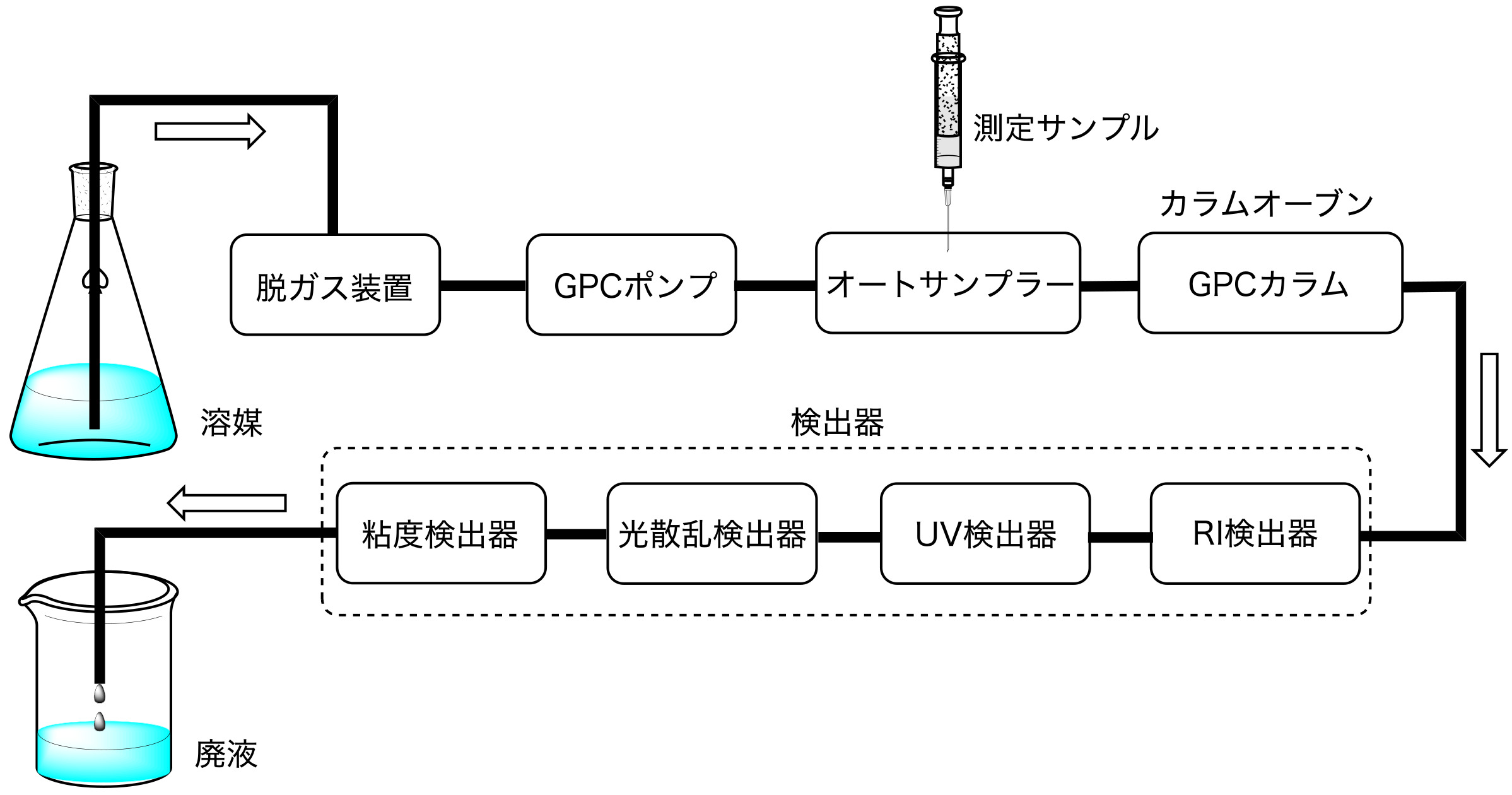
図2 GPC装置の構成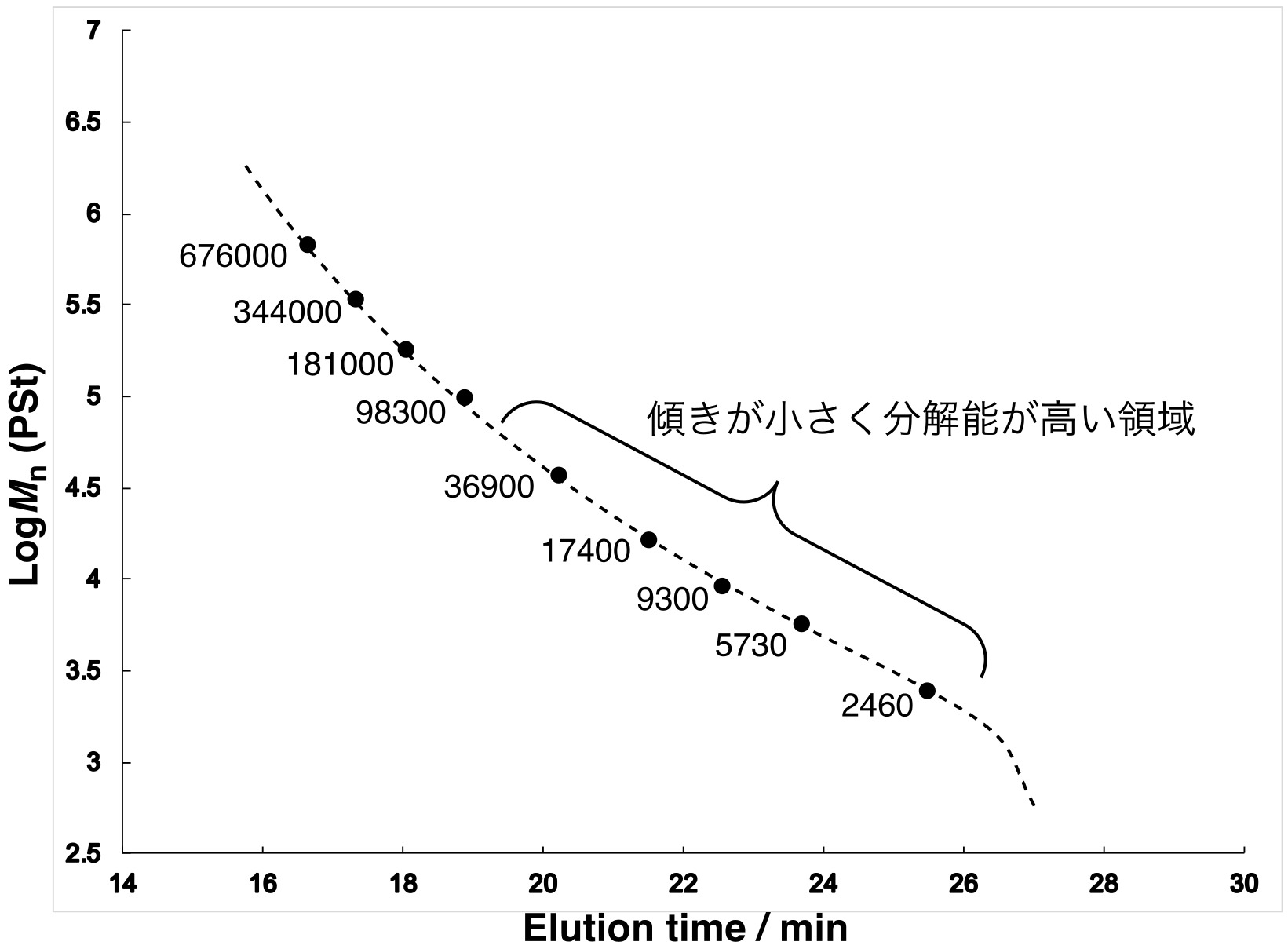
図3 典型的な較正曲線の例:ポリスチレン標準試料、THF、40℃、1mL/min
測定条件:
基本的に測定溶媒に溶解する高分子が対象となります。測定分子量範囲は数百から数百万とされ、適切な分子量領域の分離ができる孔径のカラムを使用することが重要となります。広い分子量領域の分離を行うためにカラムを複数本接続しての測定も多く行われています。測定溶媒(移動相)には幅広い高分子を溶解させることができるテトラヒドロフラン(THF)が最も広く使用され、クロロホルム、
N,N-ジメチルホルムアミド(DMF)、ヘキサフルオロイソプロパノール、水なども溶媒として使用されます。極性の大きなポリマーなどでGPCカラムへの吸着が起こる際には別種溶媒のGPCカラムを用いることで、測定が可能になる場合もあります。DMF溶媒での測定時には0.01Mの臭化リチウムを添加することで、GPCカラムへのポリマーの吸着を妨げられるようになることもあります。「高温GPC」と呼称される1,2,4-トリクロロベンゼンなど高沸点溶媒を使用するGPCでは、ポリエチレン、ポリプロピレンなどの溶解性が限られるポリオレフィンの測定も可能となります。
測定上の注意点:
GPCを実際に使用する際の注意点としては、通常の測定ではあくまでも相対分子量が求まることを理解しておく必要があります。例えば、最も汎用的なTHF溶媒のGPCでは、標準ポリスチレンによる較正曲線を使って、1,4-ポリイソプレンの分子量を測定すると、1.6倍程度に過大評価されます。すなわち、10,000の分子量のサンプルは16,000程度に相対分子量が算出されることになります。逆にポリ(2-ビニルピリジン)の場合は過小評価され、10,000の分子量が、6,000程度に算出されます。これはTHF中でのポリマーのサイズが、同分子量のポリスチレンに比較して、それぞれ広がったり(1,4-ポリイソプレン)、縮まったり(ポリ(2-ビニルピリジン))していることが反映されています。こうした場合には、前述の絶対分子量測定が可能なLS検出器やViscosity検出器を併用することが重要となります。その他の重要な知見として、同じ分子量のサンプルでも直鎖状高分子と分岐高分子(星型高分子、グラフト高分子、櫛形高分子など)では、分岐高分子の方が流体力学体積が小さくなりますので、相対分子量は過小評価されることが知られています。
1)2)3)さらには、同分子量の直鎖状高分子と環状高分子でも、流体力学体積が相対的に小さな環状高分子の方が分子量は過小評価され、実際の環化反応後に保持時間が増加する現象が観察されています。
4)
実際の使用例:
GPCによって分子量の変化が伴う様々な高分子の反応が追跡できることから、高分子合成の研究には欠かせない測定手段となっています。例として、モノマーの逐次添加によるブロック共重合、様々なグラフト(星型)高分子の合成、環状高分子の合成、解重合や平衡重合挙動、官能基の変換反応、脱保護反応など、非常に多岐に渉る反応において、分子量、分子量分布の変化を追跡できることが報告されています。一例として、メタクリル酸のジエチレングリコールエステルのポリマー側鎖を脱保護した場合のGPC流出挙動(DMF)溶媒)を示します(図4)。
5)トリアルキルシリル基の脱保護によるOH基への変換で原理的にはポリマーの分子量は減少しますが、GPC曲線は明らかに高分子量側に移動しています。また、極性のOH基をエステル化することで再び分子量は増加しますが、GPC曲線は低分子量側に移動しています。これらの結果は、極性のDMF溶媒中における、それぞれのポリマーのサイズ(流体力学体積)を反映しています。いずれのポリマーも狭い分子量分布を保っており、2回の高分子反応中にポリマーの架橋や主鎖切断などの副反応は起こっていないことが、GPC測定から強く示唆されます。一方、分子間の副反応などの進行に伴い、分子量分布の広がりがGPC測定において顕著に観察される例もあります。
6)
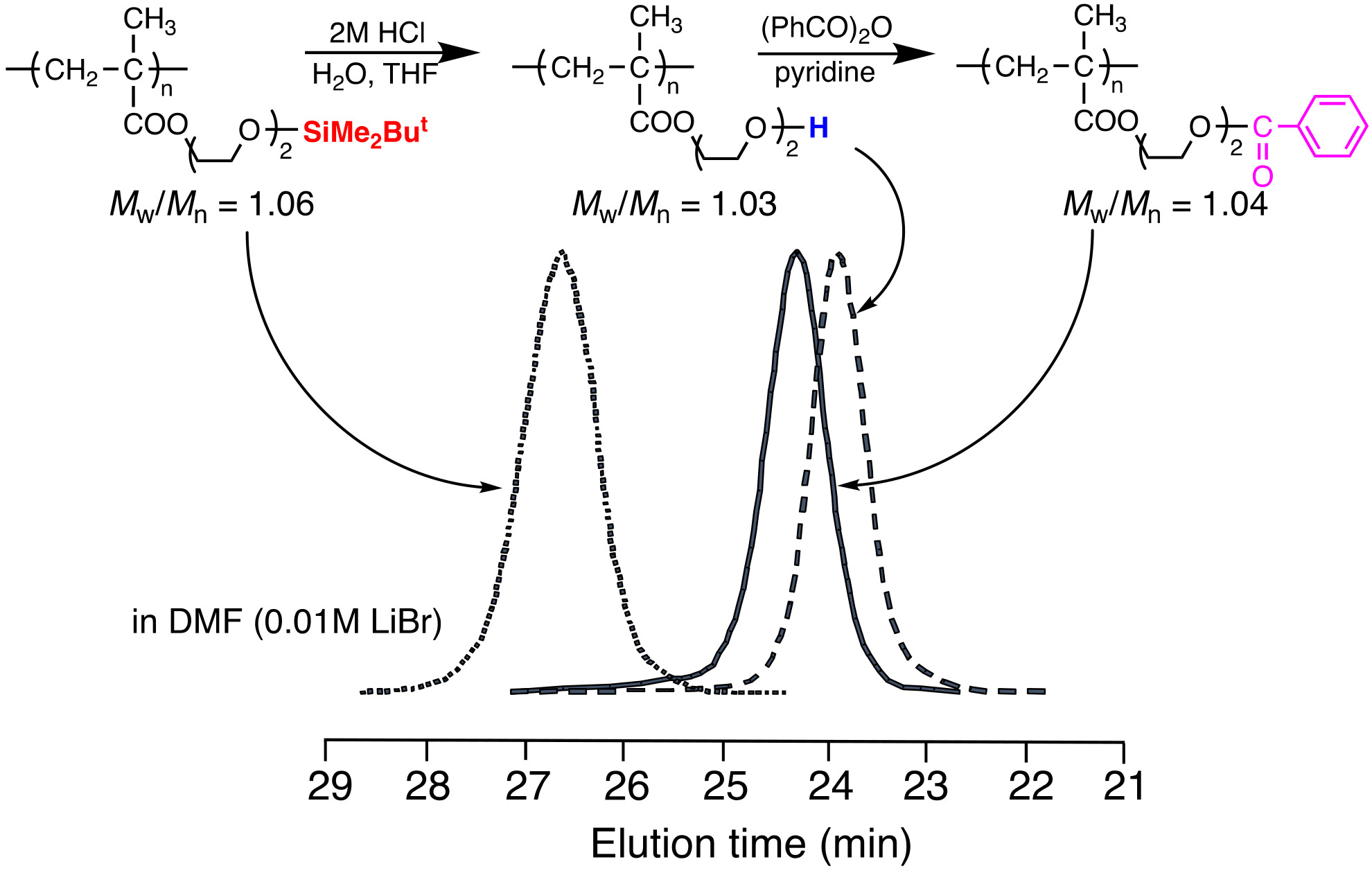 図4 ポリ(メタクリル酸ジエチレングリコール)類の側鎖末端の脱保護反応によるGPC曲線の変化
図4 ポリ(メタクリル酸ジエチレングリコール)類の側鎖末端の脱保護反応によるGPC曲線の変化
参考文献
1) A. Hirao, A. Matsuo, T. Watanabe, Macromolecules 38, 8701-8711 (2005).
2) A. Hirao, K. Murano, A. Abouelmagd, M. Uematsu, S. Ito, R. Goseki, T. Ishizone, Macromolecules 44, 3302-3311 (2011).
3) R. Goseki, S. Ito, E. Akemine, A.Hirao, Polym. Chem. 7, 6147-6280 (2016).
4) H. Oike, H. Imaizumi, T. Mouri, Y. Yoshioka, A. Uchibori, Y. Tezuka, J. Am. Chem. Soc. 122, 9592-9599 (2000).
5) T. Ishizone, S. Han, S. Okuyama, S. Nakahama, Macromolecules 36, 42-49 (2003).
6) K. Takahata, S. Uchida, R. Goseki, T. Ishizone, Polym. Chem. 10, 3951-3959 (2019).
分析例・プロトコール
.jpg)


