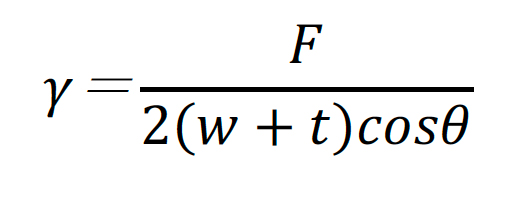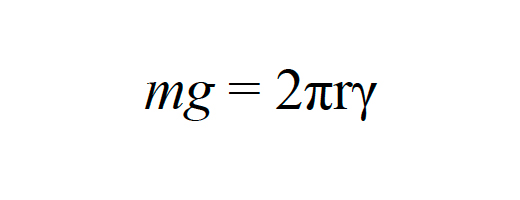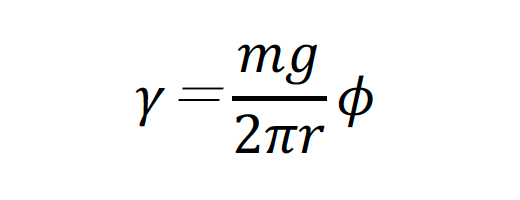執筆:遊佐真一(兵庫県立大学)
表面張力を測定することで両親媒性高分子等の臨界ミセル濃度(CMC)を決定できる
液面を縮めようとする力である表面張力は、単位面積あたりの表面エネルギーで表されます。そのため表面張力は「エネルギー/面積」の次元を持ちますが、一般的には「力/長さ」の次元で表され、mN/m(ミリニュートン毎メートル)という単位が使用されます。水に両親媒性物質を溶かすと、気―液界面に吸着して表面張力は低下します。この現象を利用して臨界ミセル濃度(CMC)を決定できます。
測定できること
表面張力 / 表面自由エネルギー / 臨界ミセル濃度(CMC)
原理
水の表面は液体と気体の境目、つまり界面となります。界面の外側は水分子どうしの結合が切れて存在しないか、結合が著しく少なくなります。一方、液の内側方向の結合は強いため、表面にある水分子は内側に引かれます。内部の水分子が表面をつくるには、この内側に向かう力を打ち消す必要があります(図1)。気―液界面には、このように表面エネルギーが存在します。表面エネルギーはなるべく小さくなろうとするため、表面積が最小の球になろうとします。つまり液体の表面張力は、液面を縮めようとする力です。表面張力はこのように考えられた量なので、単位面積あたりの表面エネルギーと定義されます。そのため表面張力は、「エネルギー/面積」の次元を持ちますが、一般的には「力/長さ」の次元で表されます。「エネルギー/面積」で考えた表面張力は表面自由エネルギーと呼ばれます。表面張力の単位は、国際単位系(SI)ではmN/m(ミリニュートン毎メートル)を、CGS単位系ではdyn/cm(ダイン毎センチメートル)を用います。水銀などの液体の金属を除けば、水は全ての液体の中で最も表面張力が大きく、常温で約72.7mN/mです。水銀の表面張力は約480mN/mです。また有機溶媒である
n-ヘキサンおよびアセトンなどの表面張力は、それぞれ18.4と23.3mN/mです。温度が上昇すると熱運動により分子間の凝集エネルギーが小さくなるため、表面張力は低下します。
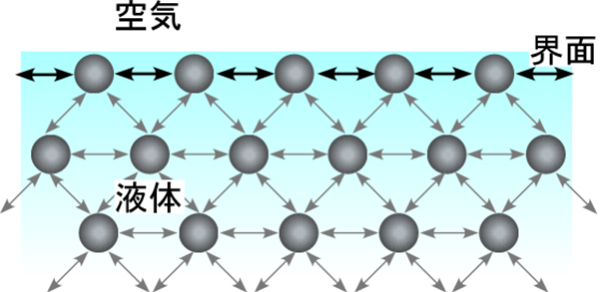 図1 液体の界面付近の状態。表面の分子は、内部の分子に比べて引力相互作用を失っている
図1 液体の界面付近の状態。表面の分子は、内部の分子に比べて引力相互作用を失っている
液体の表面張力測定法は、いろいろな方法が知られています
1)。デュ・ニュイリング(Du Nouy ring)法
2)、ウィルヘルミープレート(Wilhelmy plate)法
3)、滴重法などがあります。それぞれの測定法について以下に説明します。
デュ・ニュイリング法
デュ・ニュイリングと呼ばれる金属製(通常は白金製)のリングを液面に平行に浸して、これを垂直に引き上げ、引き上げる力を測定して表面張力を算出します。測定には、液体表面に触れたリングを液から引き離す必要があるため、表面張力の経時変化を測定することはできません。またリングを液体に漬ける必要があるので、通常は測定に30mL以上の液体を必要とします。
ウィルヘルミープレート法
薄いプレート(ウィルヘルミープレート)を液体に浸し、その際に液体がプレートを引っ張り込もうとする方向に発生する力を測定します(図2)。このとき表面張力(γ)は次式で表されます。
ここで
Fはプレートに働く力(mN)、
wはプレートの幅(m)、
tはプレートの厚み(m)、θはプレートと液体(水)との接触角を表します。θがわかっている場合は問題ありませんが、不明な場合でも液体で完全にプレートが濡れれば、θはゼロとなるので式は単純になります。そこで濡れやすい白金のプレートが良く利用されます。さらにプレートを引き上げながら測定すれば、見かけのθがゼロとなります。ウィルヘルミープレート法は、プレートを静止して測定することもできるため、動的表面張力も測定できます。プレートを液体に漬ける必要があるため、通常は測定に30mL以上の液体を必要とします。
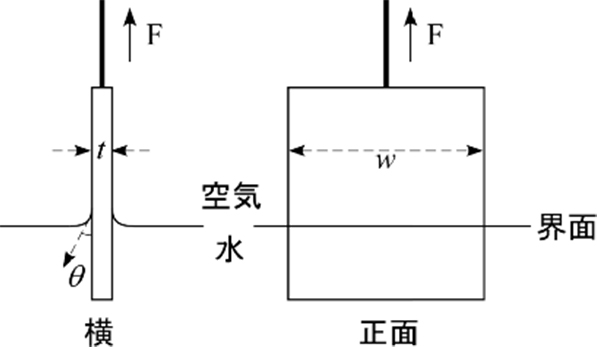 図2 ウィルヘルミープレート法の概念図
図2 ウィルヘルミープレート法の概念図
半径
r(m)の毛管から質量
m(g)の液滴が落下する瞬間を考えると(図3)、液滴にかかる重力と間の先端の周囲にわたって上向きにはたらくγが釣り合っているので、次式が成立します。
ここで
gは重力加速度(m/s
2)です。しかし実際には、毛管の先端の液滴の表面は鉛直ではなく、また生じた液滴の一部が落下するため、これを補正するためにHarkinsの補正因子ϕと呼ばれる値を用いて
4)、γを次式で求めることができます。
滴重法は、少ないサンプル量で測定できます。また溶融高分子などの粘度の高いサンプルでも表面張力を測定できます。
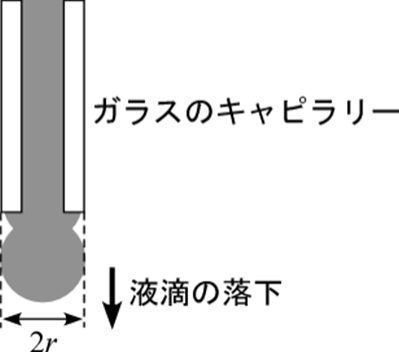 図3 滴重法の概念図
図3 滴重法の概念図
水に界面活性剤が溶解すると、界面活性剤の特異な構造のため表面張力は低下します。界面活性剤は、分子内に親水基と疎水基を持ちます。親水基は水中に存在しようとしますが、疎水基は水との接触をできるだけ避けるため、界面活性剤分子は気―液界面に集まります。つまり水の表面に界面活性剤分子が吸着することになります。そのため、水の表面は疎水基で覆われるので、表面張力の値は水の値から疎水性の油の値に近づきます(図4)。界面活性剤がある一定濃度以上になると、水の表面が界面活性剤分子で覆われるため、表面張力はほぼ一定になります。さらに液中では界面活性剤の疎水部の会合によりミセルを形成し始めます。この濃度を一般に臨界ミセル濃度(Critical Micelle Concentration: CMC)と呼びます
5)。したがって、界面活性剤や両親媒性高分子の濃度に対して、表面張力を測定することでCMCを決定できます。
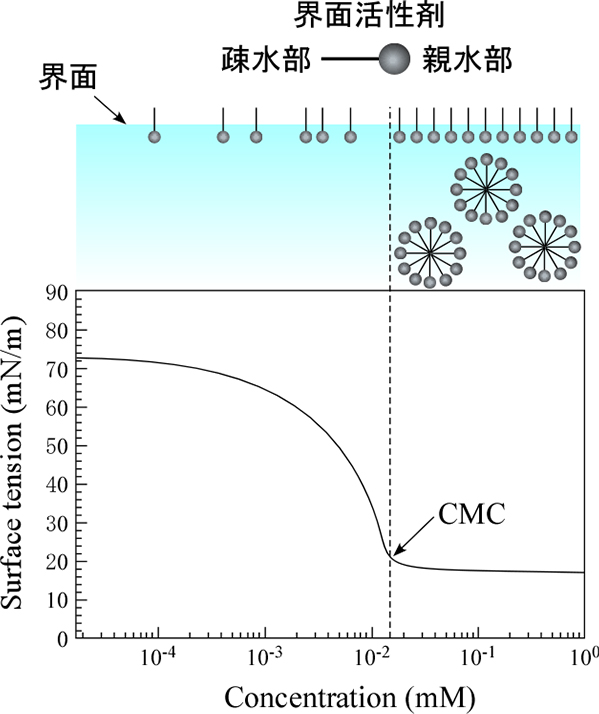 図4 表面張力による臨界ミセル濃度(CMC)の決定
図4 表面張力による臨界ミセル濃度(CMC)の決定
界面活性を持つ高分子では気-液界面への吸着に時間がかかるため、時間と共に表面張力が減少する場合があります
6)。このように時間経過に伴い平衡に向かって変化する表面張力を動的表面張力と呼びます。
参考文献
1) Mulqueen, M.; Huibers, P. D. T. In Handbook of Applied Surface and Colloid Chemistry Vol 2; Holmberg, K. Ed., Wiley, New York, 2002, pp 217–224.
2) Lunkenheimer, K.; Wantke, K. D. Colloid Polym. Sci., 1981, 259, 354–366.
3) Gaonkar, A. G.; Neuman, R. D. Colloids Surf., 1987, 27, 1–14.
4) Gunde, R.; Kumar, A.; Lehnert-Batar, S.; Maeder, R.; Windhab, E. J. J. Colloid Interface Sci., 2001, 244, 113–122.
5) Eastoe, J.; Dalton, J. S. Adv. Colloid Interface Sci., 2000, 85, 103–144.
6) Ribera, R.; Velazquez, M. M. Langmuir, 1999, 15, 6686–6691.
分析例・プロトコール